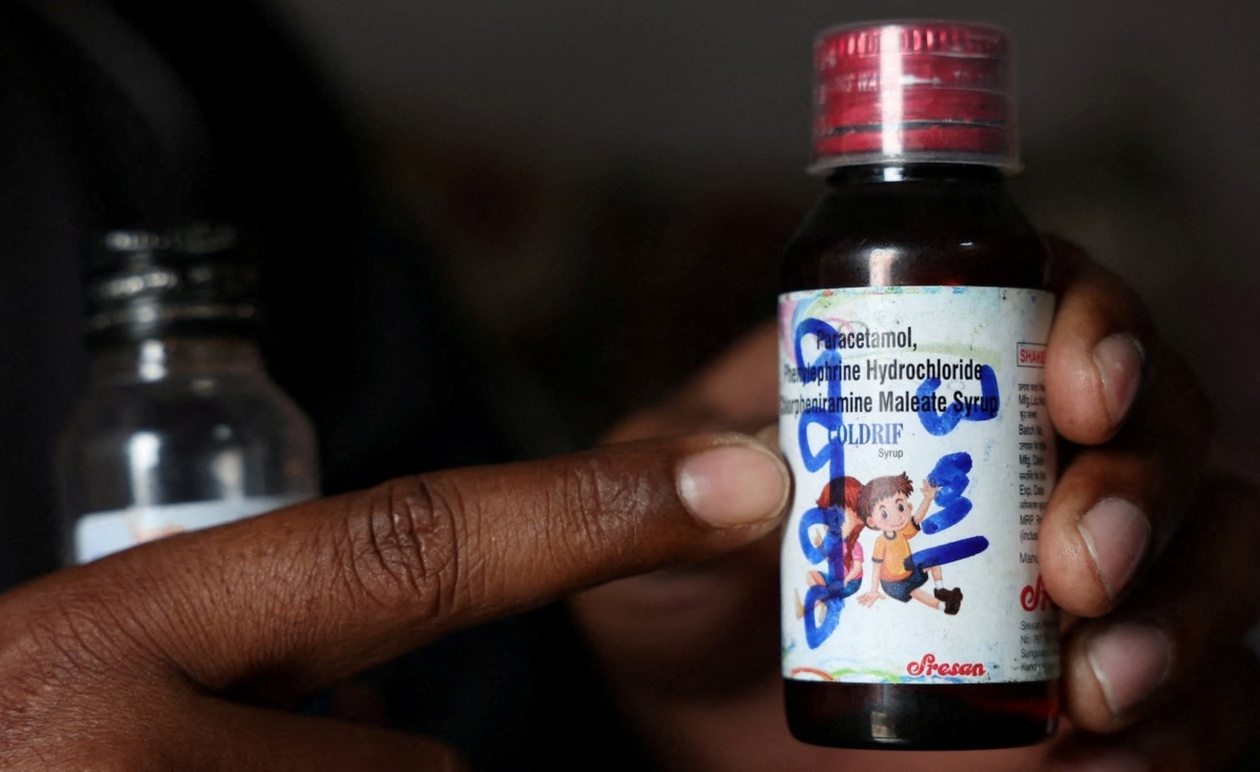
- Τουλάχιστον 24 παιδιά στην Ινδία πέθαναν από μολυσμένο σιρόπι για τον βήχα.
- Η έρευνα εστιάζει σε παραλείψεις στην αλυσίδα εφοδιασμού και σε χρήση τοξικής ουσίας (DEG).
- Η φαρμακοβιομηχανία Sresan είχε ιστορικό παραβάσεων και ελλιπών ελέγχων.
- Το περιστατικό αναδεικνύει σοβαρές αδυναμίες στον φαρμακευτικό τομέα της Ινδίας.
- Οι αρχές δεσμεύονται για αυστηρότερους ελέγχους και επιθεωρήσεις στις φαρμακευτικές εγκαταστάσεις.
Ινδικές αρχές διερευνούν εάν παραλείψεις στην αλυσίδα εφοδιασμού ενός φαρμακευτικού συστατικού ευθύνονται για τη μόλυνση σιροπιού για τον βήχα που έχει προκαλέσει τον θάνατο τουλάχιστον 24 παιδιών τους τελευταίους μήνες. Η έρευνα, που βρίσκεται σε εξέλιξη, εστιάζει στο ενδεχόμενο το διαλυτικό που χρησιμοποιήθηκε να είχε μολυνθεί με τοξική χημική ουσία, σύμφωνα με αποκλειστικές πληροφορίες του Reuters.
Αυτή η εξέλιξη έρχεται ως συνέχεια μιας σειράς θανάτων παιδιών στην Αφρική και την Κεντρική Ασία το 2022 και το 2023, οι οποίοι επίσης συνδέθηκαν με ινδικά σιρόπια για τον βήχα που περιείχαν μολυσμένα διαλυτικά. Το περιστατικό αναζωπυρώνει τις ανησυχίες για τα πρότυπα ασφαλείας στον φαρμακευτικό τομέα της Ινδίας, αξίας 50 δισεκατομμυρίων δολαρίων, και εγείρει ερωτήματα σχετικά με την αποτελεσματικότητα των ελέγχων ποιότητας που είχαν υποσχεθεί οι αρχές.
Η έρευνα και οι παραβιάσεις ασφαλείας
Τρεις αξιωματούχοι υγείας και ασφάλειας φαρμάκων από την πολιτεία Ταμίλ Ναντού δήλωσαν στο Reuters ότι πιστεύουν πως το διαλυτικό που χρησιμοποιήθηκε για την παραγωγή μιας παρτίδας του σιροπιού Coldrif μπορεί να είχε μολυνθεί με τοξική χημική ουσία περίπου την εποχή που προμηθεύτηκε στην φαρμακοβιομηχανία Sresan Pharmaceutical Manufacturer.
Η Sresan απέκτησε 50 κιλά του διαλυτικού προπυλενογλυκόλης (PG) στις 25 Μαρτίου από την τοπική εταιρεία διανομής χημικών Sunrise Biotech, η οποία το είχε αγοράσει την ίδια ημέρα από την Jinkushal Aroma, μια μικρή εταιρεία που παράγει μείγματα αρωμάτων για υγρά απορρυπαντικά.
Οι αρχές έχουν δηλώσει ότι το σιρόπι Coldrif ήταν έντονα μολυσμένο με μια γνωστή βιομηχανική τοξίνη, τη διαιθυλενογλυκόλη (DEG). Διερευνούν πώς η χημική ουσία προστέθηκε στο διαλυτικό, το οποίο χρησιμοποιείται στα σιρόπια για τον βήχα ως βάση για τη διάλυση των ενεργών συστατικών του.
Το ινδικό δίκαιο περί Φαρμάκων και Καλλυντικών απαγορεύει την πώληση και διαχείριση φαρμακευτικών συστατικών, όπως η ιατρική PG, από οντότητες που δεν διαθέτουν άδειες φαρμάκων. Ούτε η Jinkushal ούτε η Sunrise διαθέτουν τέτοιες άδειες, όπως επιβεβαίωσαν οι δύο χονδρέμποροι στο Reuters.
Οι θάνατοι και το ιστορικό της Sresan
Οι θάνατοι, οι οποίοι ξεκίνησαν τον Σεπτέμβριο, έχουν αναζωπυρώσει τις ανησυχίες για τα πρότυπα ασφαλείας στον φαρμακευτικό τομέα της Ινδίας. Η διαιθυλενογλυκόλη (DEG) συνδέεται με οξεία νεφρική βλάβη και θάνατο σε παιδιά, όταν καταναλώνεται σε υψηλά επίπεδα.
Η άδεια παραγωγής της Sresan έχει ανακληθεί και ο ιδρυτής της, G. Ranganathan, βρίσκεται υπό κράτηση. Το Reuters δεν μπόρεσε να διαπιστώσει πώς ακριβώς συνέβη η μόλυνση ή ποιος ήταν υπεύθυνος.
Αυτό που ανησυχεί τους αναλυτές και τους φορείς υγείας είναι η συστηματική φύση των παραλείψεων που αποκαλύφθηκαν. Επιθεωρήσεις που διενεργήθηκαν από την κρατική ρυθμιστική αρχή μετά τους θανάτους διαπίστωσαν εκατοντάδες «κρίσιμες» και «σημαντικές» παραβιάσεις στο εργοστάσιο της Sresan έξω από την πόλη Τσενάι, συμπεριλαμβανομένης της αποθήκευσης προϊόντων σε «ανθυγιεινές συνθήκες» και «παραποίησης δεδομένων», σύμφωνα με έκθεση της 3ης Οκτωβρίου.
Ωστόσο, η ρυθμιστική αρχή δεν συνέδεσε αυτές τις παραβιάσεις απευθείας με τους θανάτους.
Οι επιπτώσεις στον φαρμακευτικό τομέα της Ινδίας
Η υπόθεση αναδεικνύει τις ευπάθειες στην αλυσίδα εφοδιασμού φαρμακευτικών προϊόντων, ειδικά όταν εμπλέκονται ενδιάμεσοι διανομείς χωρίς τις απαραίτητες άδειες. Ο Vishwakarma της Jinkushal δήλωσε ότι έσπασε τις σφραγίδες και επανασυσκεύασε το διαλυτικό στο κατάστημά του πριν πουλήσει μέρος του στη Sunrise.
Ο Jain της Sunrise δήλωσε ότι μετέφερε στη συνέχεια τη χημική ουσία στην Sresan σε δύο δοχεία χωρίς σφραγίδες ασφαλείας, επειδή η φαρμακοβιομηχανία δεν ήθελε την αρχική ποσότητα των 215 κιλών. Εκπρόσωπος της SK picglobal, του Νοτιοκορεάτη κατασκευαστή του PG, δήλωσε ότι η εταιρεία απαγορεύει αυστηρά την επανασυσκευασία ή την αναδιανομή των προϊόντων της.
Παρά το ιστορικό της Sresan και τους κανονισμούς που απαιτούν ετήσιους ελέγχους, το εργοστάσιο της φαρμακοβιομηχανίας δεν είχε επιθεωρηθεί από το 2023, σύμφωνα με δύο κρατικούς αξιωματούχους υγείας. Ο ιδρυτής της Sresan είχε προηγουμένως φυλακιστεί για μία ημέρα το 2020 και το 2022 λόγω ανησυχιών για τα προϊόντα του, προτού του επιβληθεί πρόστιμο, σύμφωνα με τέσσερις αξιωματούχους.
Ο υπουργός Υγείας του Ταμίλ Ναντού δήλωσε επίσης τον περασμένο μήνα ότι η Sresan είχε τιμωρηθεί το 2021 και το 2023 για «μικρές παραβιάσεις», χωρίς να δώσει λεπτομέρειες. Η έλλειψη τακτικών ελέγχων και η επιμονή στις παραβάσεις υπογραμμίζουν ένα ευρύτερο πρόβλημα στην εποπτεία του κλάδου.

Η επόμενη μέρα και οι προκλήσεις
Η ινδική κυβέρνηση έχει δεσμευτεί να βελτιώσει τους ελέγχους ποιότητας στον φαρμακευτικό τομέα, ωστόσο η τρέχουσα υπόθεση αναδεικνύει την ανάγκη για αυστηρότερη εφαρμογή των κανονισμών και πιο ενδελεχή εποπτεία της αλυσίδας εφοδιασμού. Το Κεντρικό Όργανο Ελέγχου Προτύπων Φαρμάκων, το οποίο εποπτεύει τα φαρμακευτικά προϊόντα σε ομοσπονδιακό επίπεδο, παρέπεμψε τις ερωτήσεις στο Υπουργείο Υγείας της Ινδίας, το οποίο με τη σειρά του παρέπεμψε το Reuters σε κυβερνητική δήλωση που ανέφερε ότι διενεργεί περισσότερες επιθεωρήσεις σε φαρμακευτικές εγκαταστάσεις και επανεξετάζει τη παιδιατρική χρήση των σιροπιών για τον βήχα.
Η εμπιστοσύνη στα ινδικά φάρμακα, τόσο στην εγχώρια όσο και στην παγκόσμια αγορά, εξαρτάται από την ικανότητα των αρχών να διασφαλίσουν την ασφάλεια και την ποιότητα των προϊόντων.